ヒトT細胞活性・増加やCAR-Tをターゲットにした研究に最適。マウスのMHC遺伝子をノックアウトしGVHDが軽減された次世代NOGマウスモデル
ヒトの免疫システムを再現することができる動物モデルの開発は。疾患の病態生理学を研究し、新しい治療法を生み出すために重要です。次世代NOGマウスは既存のヒト免疫システム再構築モデルの限界を克服するために設計されました。
■ 次世代NOGマウスモデル NOG-ΔMHC
■ NOG-ΔMHCマウスの開発経緯
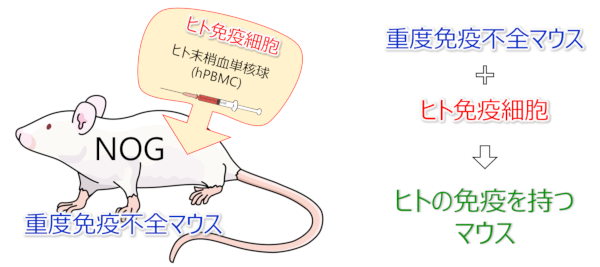
重度免疫不全マウスにヒト免疫細胞移植し、ヒト免疫を再構築
長生きができず試験期間を確保しにくい問題
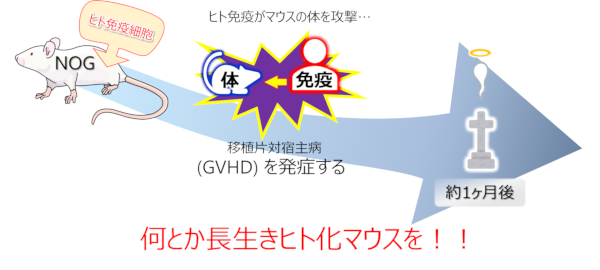
再構築されたヒト免疫がマウスの体を攻撃するため、移植片対宿主病 (Graft Versus Host Disease : GVHD)を発症し長生きすることができません。
より長生きなヒト化マウスを開発
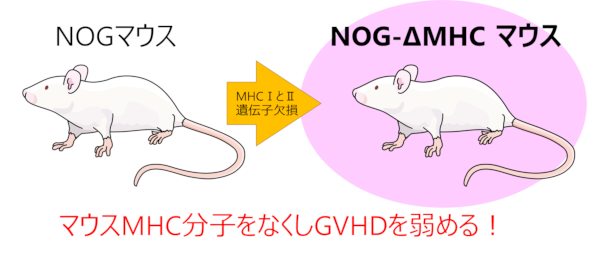
NOGマウスの優れた移植生着性に加え、移植したヒトT細胞がマウス細胞を攻撃しない/長期生存を可能にする事を目標に開発されました。NOGマウスの主要組織適合遺伝子複合体 (Major Histocompatibility Complex : MHC) のⅠとⅡの遺伝子を欠損しています。
■ ヒト末梢血単核球 (Peripheral Blood Mononuclear Cells : PBMC)でのヒト化処置
NOGマウスの場合
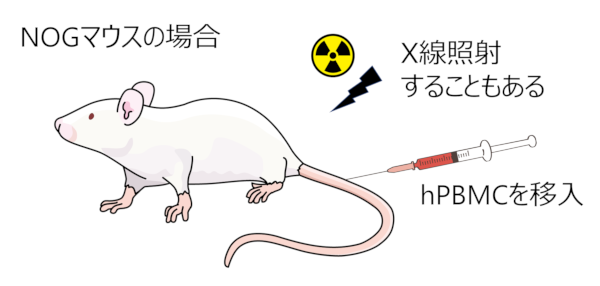
尾静脈からhPBMCを移入します。
試験系によっては、X線照射で骨髄細胞を脱落させてから、hPBMCを移入することもあります。
NOGマウスの体内
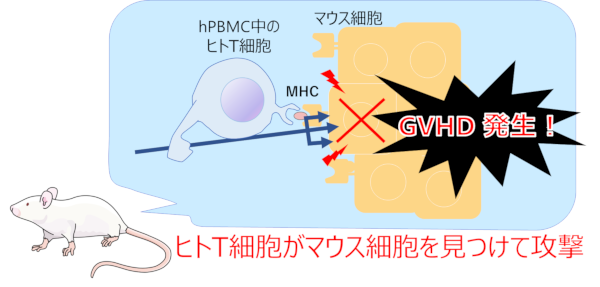
ヒトT細胞による、MHCⅠおよびⅡ分子を標識としたマウス細胞への攻撃 GVHDが発生します。
NOG-ΔMHCマウスの場合
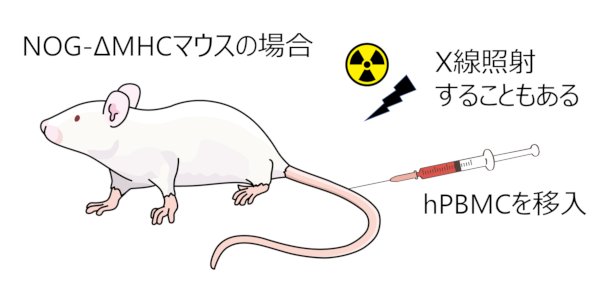
尾静脈からhPBMCを移入します。
試験系によっては、X線照射で骨髄細胞を脱落させてから、hPBMCを移入することもあります。
NOG-ΔMHCマウスの体内
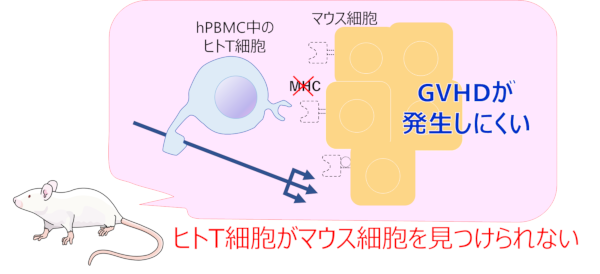
MHCⅠおよびⅡ分子が欠損しており、ヒトT細胞によるマウス細胞への攻撃 GVHDが発生しにくくなります。
NOGマウスはGVHD発症により1ヶ月程度の観察期間しかありませんでしたが、NOG-ΔMHCマウスではより長く(3ヵ月の報告例あり)観察出来る様になりました。
特徴:
- 遺伝子欠損によりヒトT細胞のマウス細胞攻撃標識となるマウスMHCⅠとⅡの発現を欠失
- hPBMC移植時、ヒトT細胞によるマウス細胞への攻撃を軽減し、GVHDを効果的に回避
- ヒトT細胞活性・増加やCAR-Tをターゲットにした研究に最適
■ NOGマウスのお問い合わせ



