日本クレアは(公財)実験動物中央研究所で開発されたNOGマウスと、その派生ラインである次世代NOGマウスのなかでも生産規模拡大の必要がある一部の系統の受託生産を行っています。
現在、複合免疫不全を呈するNOGマウスの次世代ラインナップの開発は、特に免疫研究分野に大きく加速されております。一部の系統は、日本においてインビボサイエンス株式会社より販売されており、アメリカにおいてもTaconic Biosciences社を介して販売開始され注目を集めております。
NOGマウス関連における日本クレアの生産体制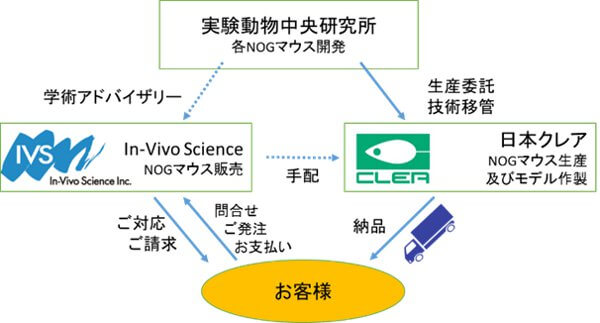
以下に販売可能な主なNOG関連系統の概要をご紹介します。
※概要説明・販売につきましてはインビボサイエンス株式会社にお問い合わせ下さい。![]()
| 目次: 1.重度免疫不全マウスの生産: ■ 次世代 NOG マウス: ■ その他: 2.ヒト化モデルマウスの作製技術: |
1. 重度免疫不全マウスの生産
NOGマウス
がん研究および再生医療等製品のがん原性試験用に需要が拡大。B細胞、T細胞、NK細胞の欠損を伴う、重度免疫不全マウスです。
がん細胞や正常細胞、iPS由来細胞など多様なヒト細胞に対して高い生着性を持たせることを目標に開発されました。近年はがん研究や再生医療・造腫瘍性試験んい需要が拡大しており、受注が増えてきています。
特徴:
- 多様な異種移植、ヒト細胞の生着が可能
- がん、感染症、免疫学、CAR-T、iPS細胞、およびヒト化免疫系移植に使用可能
原著論文:Ito M et al. Blood 2002
次世代NOGマウス
ヒトの免疫システムを再現することができる動物モデルの開発は、疾患の病態生理学を研究し、新しい治療法を生み出すために重要です。次世代NOGマウスは既存のヒト免疫システム再構築モデルの限界を克服するために設計されました。インビボサイエンス株式会社にて取り扱っておりますので、ぜひお問い合わせください。
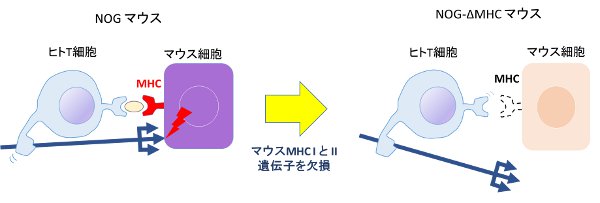
NOG-ΔMHCマウス(日本クレア生産)
ヒトT細胞活性・増加やCAR-Tをターゲットにした研究に最適。マウスのMHC遺伝子をノックアウトしGVHDが軽減された次世代NOGマウスモデルです。
概要:
NOGマウスの優れた移植生着性に加え、移植したヒトT細胞がマウス細胞を攻撃しない/長期生存を可能にする事を目標に開発されました。
NOGマウスの主要組織適合遺伝子複合体 (Major Histocompatibility Complex : MHC) のⅠとⅡの遺伝子を欠損。ヒト末梢血単核球 (Peripheral Blood Mononuclear Cells : PBMC) 移植によるヒトT細胞がマウス細胞のMHCⅠとⅡを標識とした攻撃である移植片対宿主病 (Graft Versus Host Disease : GVHD) を抑えます。
これによりGVHD発症により1ヶ月程度の観察期間しか無かったものをより長く(3ヵ月の報告例あり)観察出来る様になっています。
特徴:
- 遺伝子欠損によりヒトT細胞のマウス細胞攻撃標識となるマウスMHCⅠとⅡの発現を欠失
- hPBMC移植時、ヒトT細胞によるマウス細胞への攻撃を軽減し、GVHDを効果的に回避
- ヒトT細胞活性・増加やCAR-Tをターゲットにした研究に最適
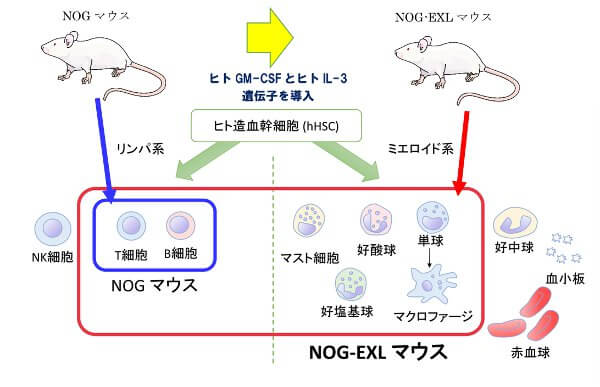
NOG-EXL マウス(日本クレア生産)
多様な免疫細胞に作用する樹状細胞を含むヒト・ミエロイド系免疫細胞をターゲットにした研究に最適。ヒトGM-CSF遺伝子とヒトIL-3遺伝子をトランスジェニックした次世代NOGモデルです。
概要:
NOGマウスの優れた移植生着性に加え、ヒト造血幹細胞 (human Hematopoietic Stem Cell : hHSC) 移植後にマウス体内にてミエロイド系免疫細胞(樹状細胞・マクロファージ等)を分化誘導させる事を目標に開発されました。
T細胞、マクロファージ、内皮細胞、線維芽細胞等の産生を促す顆粒球単球コロニー刺激因子(Granulocyte Macrophage colony-stimulating Factor : GM-CSF) 、および造血成長因子 特に骨髄系前躯細胞の増殖および生存の刺激において重要な役割を果たす Interleukin-3 (IL-3) を発現するよう、NOGマウスにヒトGM-CSFおよびヒトIL-3遺伝子を導入しています。
これによりhHSC移植後、ミエロイド系細胞の分化が優勢なヒト免疫システムの再構築が可能となりました。
特徴:
- 遺伝子導入によりヒトGM-CSFおよびヒトIL-3を発現
- このヒトGM-CSF・ヒトIL-3を発現によりhHSCの生着率が高く、ミエロイド系細胞の分化が優勢なヒト免疫システムの再構築が可能
- ミエロイド系免疫細胞産生が需要要素となる、ヒト急性骨髄性白血病移植試験に最適
NOG-FcγR KO マウス(日本クレア生産)
ヒトT細胞の免疫チェックポイントを阻害する抗体の研究に最適。マウス・マクロファージがヒト抗体を認識するFc受容体のγ鎖をコードする遺伝子をノックアウトした次世代NOGモデルです。
概要:
NOGマウスの優れた移植生着性に加え、ヒト造血幹細胞 (human Hematopoietic Stem Cell : hHSC) 移植後にマウス体内にて、投与したヒト抗体へのマウス自然免疫の影響を抑える事を目標に開発されました。
本系統ではマウスのマクロファージの表面に存在するFc受容体のγ鎖をコードする遺伝子をノックアウトして、マウスのマクロファージがヒト抗体のFc領域を認識する機能を欠損させました。
これによりマウス自然免疫を減弱させ、ヒト抗体機能の評価を効果的にシミュレーションすることができるようになりました。
特徴:
- ヒト抗体のFc領域を認識するマウスのマクロファージの機能を欠失
- マウス体内でヒト抗体機能を評価可能
- ヒトT細胞の免疫チェックポイントを阻害する抗体の研究に最適
NOG-hIL-15 Tg マウス
ヒトNK細胞をターゲットにしたがん免疫医療や、抗体依存性細胞傷害 (ADCC) 活性を用いたがん免疫治療の研究に最適。ヒトIL-15遺伝子をトランスジェニックした次世代NOGモデルです。

概要:
NOGマウスの優れた移植生着性に加え、成熟したヒトNK細胞(Natural Killer cell:NK cell)を移植後にマウス体内にて、ヒトNK細胞を長期維持・増殖させる事を目標に開発されました。
NK細胞の分化に重要な役割を果たすInterleukin-15 (IL-15) を発現するよう、NOGマウスにヒトIL-15遺伝子をトランスジェニックしました。
これにより、ヒトNK細胞活性化や抗体依存性細胞傷害(Antibody-Dependent-Cellular-Cytotoxicity:ADCC)活性でのがん免疫治療の研究が可能になりました。
特徴:
- 遺伝子導入によりヒトIL-15を発現
- ヒトIL-15を発現により成熟したヒトNK細胞細胞の移植後、長期維持・増殖可能
- NK細胞活性化やADCC活性でのがん免疫治療の研究が可能
その他:
NOG-hIL-2 Tgマウス
ヒトNK細胞をターゲットにしたがん免疫医療や、抗体依存性細胞傷害(ADCC)活性を用いたがん免疫治療の研究に最適。ヒトIL-2遺伝子をトランスジェニックした次世代NOGモデルです。

概要:
NOGマウスの優れた移植生着性に加え、成熟したヒト造血幹細胞 (human Hematopoietic Stem Cell:hHSC) 移植後にマウス体内にて、ヒトNK細胞(Natural Killer cell:NK cell)を分化誘導・活性化する事を目標に開発されました。
NK細胞の分化に重要な役割を果たすInterleukin-2 (IL-2) を発現するよう、NOGマウスにヒトIL-2遺伝子をトランスジェニックしました。
これにより、ヒトNK細胞活性化や抗体依存性細胞傷害(Antibody-Dependent-Cellular-Cytotoxicity:ADCC)活性でのがん免疫治療の研究が可能になりました。
特徴:
- 遺伝子導入によりヒトIL-2を発現
- ヒトIL-2を発現によりヒトHSCの移植後、NK細胞の分化誘導が可能
- NK細胞活性化やADCC活性でのがん免疫治療の研究が可能
NOG-hIL-6 Tgマウス
腫瘍内浸潤マクロファージ(TAM)の研究に最適。ヒトIL-6遺伝子をトランスジェニックした次世代NOGモデルです。

概要:
NOGマウスの優れた移植生着性に合わせ、ヒト造血幹細胞 (human Hematopoietic Stem Cell:hHSC) 移植後にマウス体内にて、ヒト単球およびマクロファージを分化誘導し、抗腫瘍免疫を制御して腫瘍の血管新生と転移を促進する腫瘍内浸潤マクロファージ(Tumor-Associated Macrophage:TAM)を研究することを目標に開発されました。
炎症性・抗炎症性サイトカイン両方に作用するInterleukin-6 (IL-6) を発現するよう、NOGマウスにヒトIL-6遺伝子をトランスジェニックしました。
これにより、ヒト単球が分化誘導され、ヒト腫瘍内部に浸潤したヒトマクロファージを効果的に観察することが可能になりました。
特徴:
- 遺伝子導入によりヒトIL-6を発現
- ヒト単球が分化誘導され、ヒト腫瘍内に浸潤したTAMを観察可能
- ヒトマクロファージが重要要素となる、ヒト多発性骨髄移植研究に最適
TK-NOGマウス
ヒト肝細胞移植に特化したマウス:肝臓ヒト化・肝細胞生着

概要:
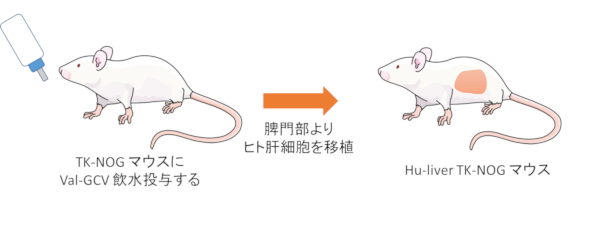
NOGマウスの優れた移植生着性に合わせ、ヒト肝細胞移植によるマウス体内でのヒト肝臓再構築を目標に開発されました。
アルブミン遺伝子のエンハンサー/プロモーター支配下で、NOGマウスの肝臓に自らをアポトーシスにより細胞を死に至らしめる「自殺遺伝子」と言われるHerpes Simplex Virus-1 Thymidine Kinase (HSV-TK) を発現する遺伝子が導入されています。
更にガンシクロビル投与によって肝臓特異的な障害を誘導し、その後初代ヒト肝細胞を脾臓門脈経由で移植してヒト肝臓を再構築、Hu-liver TK-NOGマウスを作ります。
特徴:
- NOGマウスの高い移植生着性に加えて遺伝子改変 (Tg) により肝臓特異的障害を誘導可能であるため、Hu-liverマウスを作製可能
- Tgにて肝臓特異的に単純ヘルペスウイルスのチミジンキナーゼ (TK) を発現
- 初代ヒト肝細胞移植にてヒト肝臓再構築
2.ヒト化モデルマウスの作製技術
日本クレアでは (公財) 実験動物中央研究所より技術移管され、NOGマウスおよび次世代NOGマウスの免疫をヒト化したhuNOGマウス、TK-NOGマウスの肝臓をヒト化したHu-liver TK-NOGマウスを作製しております。
huNOGマウス作製方法
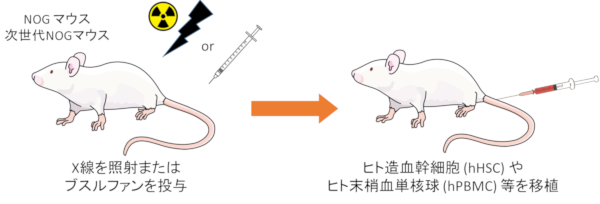
Hu-liver TK-NOG マウス作製方法